Gemita 1g - Thuốc trị ung thư kết hợp hiệu quả của Ấn Độ
Liên hệ
Chính sách khuyến mãi
Dược sỹ tư vấn 24/7.
Khách hàng lấy sỉ, sll vui lòng liên hệ call/Zalo để được cập nhật giá
Sản phẩm chính hãng, cam kết chất lượng.
Kiểm tra hàng trước khi thanh toán.
Vận chuyển toàn quốc: 25.000đ/đơn (< 2kg)
Thông tin dược phẩm
Nhà sản xuất:
Số đăng ký:
VN-21384-18
Hoạt chất:
Hoạt chất/Hàm lượng:
Hộp 1 lọ x 1g
Hạn sử dụng:
Gemcitabin (dưới dạng Gemcitabin HCl) - 1g
Công ty đăng ký:
24 tháng
Xuất xứ:
Ấn Độ
Đóng gói:
Hộp 1 lọ
Dạng bào chế:
Bột pha tiêm/truyền
Video
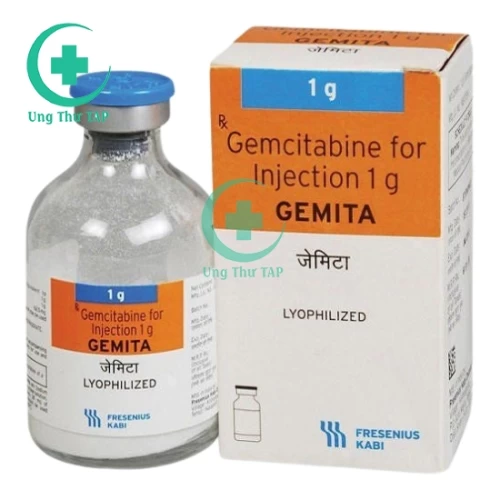
Gemita 1g là thuốc gì?
- Gemita 1g là thuốc điều trị ung thư bàng quang tại chỗ tiến triển hoặc di căn khi kết hợp với cisplatin, thuốc còn kết hợp với một số thuốc khác trong điều trị ung thư buồng trứng, ung thư vú. Ngoài ra, Gemita 1g còn được chỉ định điều trị ung thư biểu mô tuyến tụy giai đoạn cuối, ung thư bàng quang, ung thư phổi. Dưới đây, Ungthutap.com sẽ cung cấp các thông tin chi tiết nhất về công dụng, chỉ định của thuốc, liệu dùng & cách dùng cụ thể cùng với một số thông tin liên quan khác về thuốc.
Dạng bào chế
- Bột đông khô pha dung dịch tiêm truyền tĩnh mạch.
Quy cách đóng gói
- Hộp 1 lọ.
Thành phần – Nồng độ/hàm lượng
- Gemcitabin (dưới dạng Gemcitabin HCl) - 1g.
Thông tin về hoạt chất
- Dược lực học và cơ chế tác dụng:
- Gemcitabin có tác động đặc hiệu theo pha trên chu trình tế bào, chủ yếu diệt tế bào ung thư ở pha s (pha tổng hợp ADN) và ngăn chặn tế bào đang phân chia chuyển từ pha s sang pha G1. Gemcitabin được chuyển hóa ở bên trong tế bào bởi enzym nucleosid kinase để chuyển thành dẫn chất nucleosid diphosphat (dFdCDP) và triphosphat (dFdCTP) có hoạt tính. Tác động trên tế bào ung thư của gemcitabln được cho là tác động phối hợp của 2 dạng dẫn chất nucleosid diphosphat và triphosphat, từ đó gây ức chế tổng hợp ADN. Đầu tiên, gemcitabin diphosphat ức chế ribonucleotid reductase xúc tác cho phản ứng tạo deoxynucleosid triphosphat, cần cho sự tổng hợp ADN. Sự ức chế enzym này bởi nucleosid diphosphat làm giảm nồng độ deoxynucleotid, kể cả dCTP. Sau đó, gemcitabin triphosphat cạnh tranh với dCTP trong việc tích hợp vào ADN. Việc giảm nồng độ dCTP nội bào (do tác động của diphosphat) làm tăng sự tích hợp gemcitabin triphosphat vào phân tử ADN. Sau khi gemcitabin nucleotld được tích hợp vào ADN, chỉ có thêm 1 nucleotid được gắn vào phân tử ADN. Sau đó, sự tổng hợp ADN bị ức chế. Enzym DNA polymerase epsilon không có khả năng loại trừ gemcitabin nucleotid và sửa chữa chuỗi ADN hình thành. Trong dòng tế bào dạng nguyên bào lympho CEM T, gemcitabin gây phân mảnh ADN trong nhân, và đây chính là một trong những đặc điểm của quá trình chết tế bào.
- Dược động học:
- Dược động học của gemcitabin được khảo sát trên 353 bệnh nhân, 121 phụ nữ và 232 nam giới dao động từ 29 đến 79 tuổi. Trong số nhũng bệnh nhân này, khoảng 45% bệnh nhân ung thư phổi không phải tế bào nhỏ và 35% bệnh nhân ung thư tuyến tụy. Các thông số dược động học sau đây thu được với liều từ 500 đến 2592 mg/m2 được truyền từ 0,4 đến 1,2 giờ.
- Nồng độ đỉnh trong huyết tương (thu được trong vòng 5 phút sau khi truyền) là 3,2 đến 45,5 mcg/ml. Nồng độ trong huyết tương của hợp chất gốc sau liều 1000 mg/m2 khoảng 30 phút lớn hơn 5 mcg/ml trong khoảng 30 phút sau khi truyền xong và hơn 0,4 mcg/ml sau 1 giờ truyền.
- Phân bố
- Thể tích phân bố của khoang trung ương là 12,4 L/m2 ở nữ giới và 17,5 L/m2 ở nam giới (biến động giữa các cá thể là 91,9%). Thể tích phân bố của khoang ngoại vi là 47,4 L/m2. Thể tích phân bố của khoang ngoại vi không bị ảnh hưởng bởi giới tính. Sự gắn kết protein huyết tương được coi là không đáng kể.
- Thời gian bán thải từ 42 đến 94 phút tùy thuộc vào độ tuổi và giới tính. Đối với liều khuyến cáo, gemcitabin được đào thải trong vòng 5 đến 11 giờ khi bắt đầu truyền. Gemcitabin không tích tụ khi dùng liều mỗi tuần một lần.
- Chuyển hóa
- Gemcitabin được chuyển hóa nhanh chóng bằng cytidin deaminase trong gan, thận, máu và các mô khác. Chuyển hóa nội bào của gemcitabin tạo ra gemcitabin mono-, di- và tri-phosphat (dFdCMP, dFdCDP và dFdCTP) trong đó dFdCDP và dFdCTP được coi là có hoạt tính. Những chất chuyển hóa nội bào này không được phát hiện trong huyết tương hoặc nước tiểu. Chất chuyển hóa chính, 2′-deoxy-2 2′-difluorouridin (dFdU) không có hoạt tính và được tìm thấy trong huyết tương và nước tiểu.
- Thải trừ
- Tỷ lệ độ thanh thải hệ thống dao động từ 29,2 L/giờ/m2 đến 92,2 L/giờ/m2, phụ thuộc vào giới tính và độ tuổi (biến động giữa các cá thể là 52,2%). Độ thanh thải ở nữ giới thấp hơn ở nam giới 25%. Độ thanh thải ở cả nam giới và nữ giới dường như cũng giảm theo độ tuổi. Khi sử dụng liều khuyến cáo 1000 mg/nr truyền trong 30 phút, việc giảm độ thanh thải ở nữ giới và nam giới không dẫn đến việc phải giảm liều dùng.
- Có ít hon 10% thuốc được đào thải qua nước tiểu ở dạng không đổi. Độ thanh thải ở thận là từ 2 đến 7 L/giờ/m2. Trong 1 tuần sau khi dùng thuốc, 92-98% liều gemcitabin đã dùng được đào thải, 99% qua thận, chủ yếu ở dạng dFdU và 1% liều được thải trừ qua phân.
Tác dụng - Chỉ định của thuốc Gemita 1g
- Gemcitabin được chỉ định để điều trị ung thư bàng quang tại chỗ tiến triển hoặc di căn khi kết hợp với cisplatin.
- Gemcitabin được chỉ định để điều trị bệnh nhân ưng thư biểu mô tuyến tụy tại chỗ tiến triển hoặc di căn.
- Gemcitabin kết hợp với cisplatin được chỉ định trong điều trị khởi đầu cho những bệnh nhân ung thư phổi không phải tế bào nhỏ ở giai đoạn tiến triển tại chỗ hoặc di căn. Gemcitabin đơn trị liệu có thể được xem xét ở bệnh nhân cao tuổi hoặc những bệnh nhân có chỉ số toàn trạng là 2.
- Gemcitabin kết hợp với carboplatin được chỉ định để điều trị cho bệnh nhân ung thư buồng trứng ở giai đoạn tiến triển hoặc di căn, ở những bệnh nhân bị tái phát trở lại ít nhất 6 tháng sau khi kết thúc phác đồ hóa trị với dẫn chất platin.
- Gemcitabin kết hợp với paclitaxel, được chỉ định để điều trị cho các bệnh nhân ung thư vú tái phát tại chỗ hoặc di căn sau khi thất bại với phác đồ hóa trị hỗ trợ có nhóm anthracyclin, trừ khi anthracyclin bị chống chỉ định trên lâm sàng.
Chống chỉ định của thuốc Gemita 1g
- Bệnh nhân mẫn cảm với bất kỳ thành phần nào của thuốc.
- Phụ nữ cho con bú
Liều lượng - Cách dùng của thuốc Gemita 1g
- Cách dùng:
- Gemita chỉ được sử dụng để tiêm truyền tĩnh mạch
- Gemcitabin được dung nạp tốt qua đường tiêm truyền tĩnh mạch.
- Nếu xảy ra thoát mạch, cần ngừng truyền ngay lập tức và bắt đầu truyền lại vào một mạch máu khác. Bệnh nhân cần được theo dõi cẩn thận sau khi truyền.
- Thận trọng khi pha chế và truyền thuốc
- Cần thận trọng khi pha chế dung dịch gemcitabin để truyền cho bệnh nhân. Xử lý dung dịch khi pha phải được làm trong hộp an toàn và phải dùng áo bảo hộ và găng tay. Nếu không có hộp an toàn, thiết bị nên được bổ sung bằng mặt nạ và kính bảo vệ. Nếu dung dịch gemcitabin tiếp xúc với da hoặc niêm mạc, phải lập tức rửa kỹ vùng da đó với xà phòng và nước hoặc rửa niêm mạc bị tiếp xúc với nhiều nước. Nếu dung dịch gemcitabin tiếp xúc với mắt, điều này có thể gây kích ứng nghiêm trọng. Đôi mắt cần được rửa sạch ngay và triệt để với nước, cần tuân thủ quy định về xử lý và tiêu hủy đối với các thuốc trị ung thư.
- Sử dụng dung dịch acid sulfuric 0,5M và kali permanganat 0,1M trong 2 giờ để trung hòa thuốc nếu thuốc bị đổ hay rơi vãi ra bên ngoài.
- Pha dung dịch tiêm truyền tĩnh mạch
- Khuyến cáo sử dụng dung môi là NaCl 0,9% để pha dung dịch tiêm truyền gemcitabin. Do đặc tính hòa tan, nồng độ tối đa khi pha dung dịch gemcitabin là 40 mg/ml. Khi pha chế dung dịch có nồng độ cao hơn 40 mg/ml, cần tránh trường hợp thuốc không hòa tan hoàn toàn có thể xảy ra.
- Sử dụng kỹ thuật pha chế vô khuẩn để pha dung dịch gemcitabin tiêm truyền tĩnh mạch.
- Để pha chế, thêm 5 ml dung dịch NaCl 0,9% pha tiêm vào ống thuốc 200 mg hoặc thêm 25 ml dung dịch NaCl 0,9% pha tiêm vào ống thuốc 1 g. Lắc đều để hòa tan. Cách pha chế này sẽ tạo được dung dịch gemcitabin có nồng độ là 38 mg/ml, tổng thể tích sau khi pha tương ứng là 5,26 ml và 26,3 ml. Sau khi rút hết dung dịch trong lọ ra sẽ thu được dung dịch chứa tương ứng là 200 mg hoặc 1 g. Có thể truyền dung dịch đã pha với một lượng thuốc thích hợp hoặc có thể tiếp tục pha loãng thêm bằng dung dịch NaCl 0,9% pha tiêm. Dung dịch gemcitabin sau khi pha để tiêm truyền phải trong suốt, không màu hoặc có màu vàng rơm nhạt.
- Cần kiểm tra dung dịch pha chế bằng mắt để phát hiện các tiểu phân không tan hoặc sự biến màu trước khi truyền thuốc cho bệnh nhân. Nếu có tiểu phân không tan hoặc có sự biến màu, không truyền dung dịch này cho bệnh nhân. Hủy bỏ phần dung dịch thừa. Không được để dung dịch gemcitabin đã pha trong tủ lạnh vì có thể gây kết tinh.
- Liều dùng:
- Ung thư bàng quang
- Sử dụng phối hợp
- Liều khuyến cáo của gemcitabin là 1000 mg/m2, tiêm truyền tĩnh mạch trong 30 phút vào các ngày 1, 8 và 15 trong mỗi chu kỳ 28 ngày. Cisplatin được sử dụng liều khuyến cáo là 70 mg/m2 vào ngày 1 sau khi truyền gemcitabin hoặc vào ngày 2 của mỗi chu kỳ 28 ngày. Lặp lại chu kỳ sau mồi 4 tuần. Có thể giảm liều sau mỗi chu kỳ hoặc trong chu kỳ tùy theo mức độ độc tính gặp phải ở bệnh nhân.
- Ưng thư tuyến tụy
- Liều khuyến cáo của gemcitabin là 1000 mg/m2, tiêm truyền tĩnh mạch trong 30 phút, lặp đi lặp lại mỗi tuần một lần trong vòng 7 tuần, sau đó nghỉ 1 tuần. Các chu kỳ tiếp theo cũng bao gồm truyền tĩnh mạch 1 lần mỗi tuần trong 3 tuần liên tiếp rồi nghỉ 1 tuần. Có thể giảm liều sau mỗi chu kỳ hoặc trong chu kỳ tùy theo mức độ độc tính gặp phải ở bệnh nhân.
- Ung thư phổi không phải tế bào nhỏ
- Đơn trị liệu
- Liều khuyến cáo của gemcitabin là 1000 mg/m2, tiêm truyền tĩnh mạch trong 30 phút, lặp đi lặp lại mỗi tuần một lần trong vòng 3 tuần, sau đó nghỉ 1 tuần. Chu kỳ 4 tuần này nên được lặp lại. Có thể giảm liều sau mỗi chu kỳ hoặc trong chu kỳ tùy theo mức độ độc tính gặp phải ở bệnh nhân.
- Sử dụng phối hợp
- Liều khuyến cáo của gemcitabin là 1250 mg/m2 diện tích bề mặt cơ thể, tiêm truyền tĩnh mạch trong 30 phút vào ngày 1 và 8 của chu kỳ điều trị (21 ngày). Có thể giảm liều sau mỗi chu kỳ hoặc trong chu kỳ tùy theo mức độ độc tính gặp phải ở bệnh nhân.
- Cisplatin được sử dụng với liều từ 75-100 mg/m2 mỗi 3 tuần một lần.
- Ung thư vú
- Sử dụng phối hợp
- Khi gemcitabin kết hợp với paclitaxel, paclitaxel được khuyến cáo dùng liều 175 mg/m2 vào ngày 1, tiêm truyền tĩnh mạch trong khoảng 3 giờ; sau đó sử dụng gemcitabin với liều 1250 mg/m2 tiêm truyền tĩnh mạch trong 30 phút vào ngày 1 và 8 của mỗi chu kỳ 21 ngày. Có thể giảm liều sau mỗi chu kỳ hoặc trong chu kỳ tùy theo mức độ độc tính gặp phải ở bệnh nhân. Bệnh nhân cần phải có số lượng bạch cầu hạt tối thiểu là 1500 x 10^6/L trước khi bắt đầu điều trị phối hợp gemcitabin + paclitaxel.
- Ưng thư buồng trứng
- Sử dụng phối hợp
- Khi gemcitabin kết hợp với carboplatin, gemcitabin được khuyến cáo dùng liều 1000 mg/m2 tiêm truyền tĩnh mạch trong 30 phút vào ngày 1 và 8 của mỗi chu kỳ 21 ngày. Sau khi dùng gemcitabin, carboplatin được dùng vào ngày 1 phù hợp với vùng đích dưới đường cong (AUC) là 4,0 mg/ml/phút. Có thể giảm liều sau mỗi chu kỳ hoặc trong chu kỳ tùy theo mức độ độc tính gặp phải ở bệnh nhân.
- Sử dụng ở nhóm đối tượng đặc biệt:
- Bệnh nhân suy thận hoặc suy gan
- Nên sử dụng gemcitabin thận trọng ở bệnh nhân suy gan hoặc suy thận vì không có đủ dữ liệu lâm sàng để đưa ra các khuyến cáo rõ ràng cho những bệnh nhân này (xem mục Cảnh báo và thận trọng khi dùng thuốc).
- Người cao tuổi (> 65 tuổi)
- Gemcitabin được dung nạp tốt ở bệnh nhân trên 65 tuổi. Không có bằng chứng nào cho thấy cần điều chỉnh liều lượng ở người cao tuổi, trừ những khuyến cáo chung cho tất cả các bệnh nhân (xem mục Cảnh báo và thận trọng khi dùng thuốc).
- Bệnh nhân nhi (< 18 tuổi)
- Không khuyến cáo sử dụng gemcitabin ở trẻ em dưói 18 tuổi do không đủ dữ liệu về tính an toàn và hiệu quả.
- Bệnh nhân suy thận hoặc suy gan
- Ung thư bàng quang
Lưu ý đặc biệt, cảnh báo và thận trọng
- Độc tính trên huyết học
- Gemcitabin có thể gây ức chế tủy xương, biểu hiện bởi giảm bạch cầu, giảm tiểu cầu, thiếu máu. Nên ngừng thuốc hoặc điều chỉnh liều dùng khi thấy có biểu hiện suy tủy, tuy nhiên suy tủy thường tồn tại trong thời gian ngắn và thường không dẫn đến việc phải giảm liều và hiếm khi ngừng thuốc.
- Công thức máu có thể tiếp tục xấu đi sau khi ngừng sử dụng gemcitabin. cần thận trọng khi bắt đầu sử dụng ở bệnh nhân suy tủy. Cũng như các phương pháp điều trị gây độc tế bào khác, cần phải xem xét đến nguy cơ ức chế tủy xương khi điều trị bằng gemcitabin kết hợp với hóa trị liệu khác.
- Suy gan và suy thận
- Gemcitabin cần được sử dụng thận trọng ở bệnh nhân suy gan hoặc suy thận vì không có đủ dữ liệu lâm sàng để đưa ra các khuyến cáo rõ ràng cho những bệnh nhân này.
- Việc sử dụng Gemcitabin ở những bệnh nhân có kèm theo di căn gan hoặc tiền sử bệnh viêm gan, nghiện rượu hoặc xơ gan có thể làm trầm trọng thêm tình trạng suy gan sẵn có.
- Đánh giá chức năng thận và gan trong phòng thí nghiệm (bao gồm các xét nghiệm về virus học) nên đupc thực hiện định kỳ.
- Xạ trị đồng thời
- Sử dụng xạ trị đồng thời (sử dụng cùng lúc hoặc cách dưới 7 ngày): Độc tính đã được báo cáo (xem mục Tương tác của thuốc).
- Tiêm vắc xin sống
- Không khuyến cáo sử dụng vắc xin sốt vàng và vắc xin sống giảm độc lực ở những bệnh nhân được điều trị bằng gemcitabin (xem mục Tương tác của thuốc).
- Hội chứng não trắng có hồi phục
- Hội chứng não trắng có hồi phục (PRES – Posterior Reversible Encephalopathy Syndrome) có hậu quả nghiêm trọng đã được báo cáo ở những bệnh nhân dùng gemcitabin dưới dạng đơn trị liệu hoặc phối hợp với các thuốc điều trị hóa học khác. Tăng huyết áp và động kinh cấp tính được báo cáo ở hầu hết bệnh nhân gemcltabin mắc PRES, nhưng các triệu chứng khác như nhức đầu, hôn mê, lẫn lộn cũng có thể xảy ra. Chẩn đoán được khẳng định một cách tối ưu bởi hình ảnh cộng hưởng từ (MRI). PRES thường có thể hồi phục với các biện pháp hỗ trợ thích hợp. Gemcitabin nên được ngưng vĩnh viễn và thực hiện các biện pháp hỗ trợ, bao gồm kiểm soát huyết áp và chống động kinh, nếu PRES phát triển trong suốt quá trình điều trị.
- Bệnh tim mạch
- Do gemcitabin gây nguy cơ rối loạn về tim mạch và/ hoặc mạch máu nên cần thận trọng khi sử dụng với bệnh nhân có tiền sử rối loạn tim mạch.
- Hội chứng rỏ rỉ mao mạch: Hội chứng rò rỉ mao mạch đã được báo cáo ở những bệnh nhân dùng gemcitabin đơn trị liệu hoặc phối hợp với các thuốc điều trị hóa học khác. Tình trạng này có thể được điều trị nếu phát hiện và được quản lý hợp lý, nhưng các ca tử vong đã được báo cáo. Tình trạng này liên quan đến sự tăng trương lực mao mạch có tính hệ thống, trong đó các chất lỏng và protein từ không gian mạch máu rò rỉ vào mô kẽ. Các đặc điểm lâm sàng bao gồm sưng phù toàn thân, tăng cân, giảm albumin, hạ huyết áp, suy thận cấp và phù phổi. Nên ngưng sử dụng gemcitabin và thực hiện các biện pháp hỗ trợ nếu hội chứng rò rỉ mao mạch phát triển trong suốt quá trình điều trị. Hội chứng rò rỉ mao mạch có thể xảy ra trong các chu kỳ sau và đã được liên kết với hội chứng suy hô hấp người lớn trong các tài liệu ghi nhận.
- Độc tính trên phổi
- Độc tính trên phổi, đôi khi nghiêm trọng (như phù phổi, viêm phổi kẽ hay hội chứng suy hô hấp người lớn) đã được ghi nhận xảy ra khi sử dụng gemcitabin. Trong trường hợp có độc tính nặng trên phổi, cần cân nhắc việc ngưng điều trị gemcitabin và thực hiện các biện pháp điều trị hỗ trợ để giúp cải thiện tình trạng.
- Độc tính trên thận
- Hội chứng tan huyết tăng urê máu: Các kết quả lâm sàng phù hợp với hội chứng tan huyết tăng urê máu (HUS) ít khi được báo cáo ở bệnh nhân dùng gemcitabin (dữ liệu sau khi tiếp thị). HUS là một rối loạn có khả năng đe dọa mạng sống. Nên ngưng sử dụng gemcitabin khi có những dấu hiệu đầu tiên của bất cứ bằng chứng nào về thiếu máu tan máu với bệnh lý vi mạch, ví dụ như giảm nhanh hemoglobin kèm theo giảm tiểu cầu, tăng bilirubin huyết thanh, creatinin huyết thanh, urê máu (BUN) hoặc lactat dehydrogenase (LDH). Suy thận có thể không hồi phục nếu ngừng điều trị và có thể phải chạy thận.
- Khả năng sinh sản
- Trong các nghiên cứu về khả năng sinh sản, gemcitabin gây ra sự giảm sinh tinh ở chuột đực. Vì vậy, nam giới được điều trị bằng gemcitabin không nên có con trong và sau 6 tháng điều trị, đồng thời nên tìm kiếm thêm lời khuyên về bảo tồn lạnh tinh trùng trước khi điều trị vì khả năng vô sinh do điều trị bằng gemcitabin có thể xảy ra.
- Bệnh nhân nhi (< 18 tuổi)
- Không khuyến cáo sử dụng gemcitabin ở trẻ em dưới 18 tuổi do không đủ dữ liệu về tính an toàn và hiệu quả.
Sử dụng cho phụ nữ có thai hoặc đang cho con bú
- Thời kỳ mang thai:
- Không có dữ liệu về sử dụng thuốc trên phụ nữ có thai, chỉ nên dùng thuốc nếu lợi ích vượt trội so với nguy cơ. Các nghiên cứu trên động vật đã cho thấy độc tính trên sinh sản. Dựa vào các kết quả từ các nghiên cứu trên động vật và cơ chế tác dụng của gemcitabin, không nên dùng gemcitabin trong thai kỳ trừ khi cần thiết. Phụ nữ nên được khuyên không nên mang thai trong thời gian điều trị với gemcitabin. Nếu bệnh nhân có thai khi đang sử dụng thuốc, cần thông báo cho bệnh nhân tất cả những nguy cơ trên bào thai
- Thời kỳ cho con bú:
- Vẫn chưa xác định được liệu gemcitabin có bài tiết qua sữa mẹ hay không và các tác dụng bất lợi của gemcitabin trên trẻ bú sữa mẹ. Vì vậy, cần ngưng cho con bú khi đang điều trị với gemcitabin
Sử dụng cho người lái xe và vận hành máy móc
- Gemcitabin có thể gây cảm giác buồn ngủ, đặc biệt nếu bệnh nhân sử dụng đồ uống chứa cồn. Khuyến cáo chỉ lái xe và vận hành máy móc nếu đảm bảo chắc chắn không có cảm giác buồn ngủ.
Tác dụng phụ của thuốc Gemita 1g
- Tác dụng phụ rất thường gặp:
- Bệnh nhân bị thiếu máu, giảm bạch cầu, giảm tiểu cầu, khó thở, nôn ói, buồn nôn.
- Bệnh nhân bị phát ban do dị ứng da thường kết hợp với ngứa, rụng tóc, tăng men gan (AST và ALT) và Phosphatase kiềm, tiểu máu, Protein niệu nhẹ.
- Bệnh nhân có triệu chứng giống cúm – phố biển nhất là sốt, đau đầu, ớn lạnh, đau cơ, suy nhược và chán ăn, ho, viêm mũi, mệt mỏi, đổ mồ hôi và khó ngủ.
- Bệnh nhân có các triệu chứng: phù ngoại biên, bao gồm cả phủ mặt, phù thường có thể hồi phục sau khi ngừng điều trị với thuốc.
- Tác dụng phụ thường gặp:
- Bệnh nhân có triệu chứng sốt giảm bạch cầu, chán ăn, đau đầu, mất ngủ, buồn ngủ, ho, viêm mũi, tiêu chảy, táo bón, viêm loét miệng, ngứa, ra mồ hôi, lưng, đau cơ, sốt, suy nhược, ớn lạnh.
- Tác dụng phụ ít gặp:
- Bệnh nhân có dấu hiệu viêm phổi mô kẽ, co thắt phế phổi.
- Tác dụng phụ hiếm gặp:
- Nhồi máu cơ tim, hạ huyết áp, tăng Gamma-Glutamyl Transferase (GGT), loét hoặc rộ da rộng, phản ứng tại chỗ tiêm.
- Tác dụng phụ rất hiếm gặp:
- Bệnh nhân bị tăng tiểu cầu, phản ứng phản vệ, tróc da và lột da nặng.
- Tác dụng phụ không rõ:
- Bệnh nhân bị loạn nhịp tim, xuất hiện hội chứng ức chế hô hấp người lớn, bỏng tỉa xạ, dịch trong, phổi, nhiễm độc phóng xạ, viêm đại tràng thiếu máu cục bộ, suy tim, suy thận, hoại tử các ngón tay hoặc ngón chân, tổn thương gan nghiêm trọng, bao gồm cả suy gan, đột quỵ.
- Bệnh nhân phải thông báo ngay cho bác sĩ những tác dụng không mong muốn gặp phải khi dùng thuốc.
Tương tác thuốc
- Chưa có nghiên cứu tương tác thuốc đặc biệt được báo cáo
- Xạ trị
- Đồng thời (dùng đồng thời hoặc cách nhau ≤ 7 ngày) – Độc tính liên quan với điều trị đa phương pháp phụ thuộc vào nhiều yếu tố khác nhau, bao gồm liều gemcitabine, tần suất sử dụng, mức độ bức xạ, kỹ thuật dự định xạ trị, mô đích, và thể tích đích. Các nghiên cứu tiền lâm sàng và lâm sàng cho thấy gemcitabine có hoạt tính nhạy cảm với tia xạ. Trong một thử nghiệm đơn, dùng đồng thời liều gemcitabine 1000 mg/m2 với liệu pháp xạ trị ở ngực cho những bệnh nhân ung thư phổi không phải tế bào nhỏ, độc tính nghiêm trọng đáng kể, và viêm màng nhầy đe dọa tính mạng tiềm ẩn, viêm thực quản, và viêm phổi đã được quan sát thấy đặc biệt ở những bệnh nhân với thể tích xạ trị lớn [thể tích điều trị trung bình 4,795cm3]. Các nghiên cứu sau đó cho rằng đó có thể là dùng gemcitabine liều thấp đồng thời cùng xạ trị với độc tính có thể dự đoán trước được, như một nghiên cứu pha II với bệnh ung thư phổi không phải tế bào nhỏ, áp dụng xạ trị ở ngực với mức 66 Gy đồng thời với sử dụng gemcitabine (600 mg/m2, 4 lần) và cisplatin (80 mg/m2 2 lần) trong 6 tuần. Chế độ điều trị an toàn tối ưu của gemcitabine với liều trị liệu xạ trị chưa được xác định ở tất cả các loại ung thư.
- Không đồng thời (cách nhau > 7 ngày) – phân tích dữ liệu không chỉ ra bất kỳ sự tăng độc tính nào khi dùng gemcitabine nhiều hơn 7 ngày trước hoặc sau phóng xạ, ngoài phản ứng phóng xạ. Các dữ liệu cho thấy có thể bắt đầu dùng gemcitabine sau khi các ảnh hưởng cấp tính của phóng xạ đã được phục hồi hoặc ít nhất 1 tuần sau xạ trị.
- Có báo cáo về tốn thương do xạ trị trên mô đích (như viêm thực quản, viêm ruột kết và viêm phổi) liên quan đến việc dùng đồng thời và không đồng thời với gemcitabin.
- Các tương tác khác
- Vắc xin điều trị sốt vàng da và các vắc xin phòng bệnh khác không được chỉ định vì ảnh hưởng nặng tới cơ thể, có thể chết người, bệnh tật, ức chế miễn dịch rõ ràng ở bệnh nhân.
Quá liều và xử trí
- Quá liều
- Liều cao đến 5700 mg/m2 đã được truyền tĩnh mạch trong 30 phút mỗi 2 tuần với độc tính lâm sàng chấp nhận được.
- Cách xử trí khi dùng thuốc quá liều
- Không có thuốc giải độc khi quá liều gemtacibin. Trong trường hợp nghi ngờ quá liều, bệnh nhân cần được theo dõi công thức máu và áp dụng các biện pháp điều trị hỗ trợ cần thiết khác. Tích cực theo dõi để có biện pháp xử trí kịp thời.
Bảo quản
- Bảo quản ở nhiệt độ không quá 30°C. Tránh ánh sáng. Để xa tầm tay của trẻ em.
Nguồn tham khảo
- Trên đây là các thông tin cần biết về thuốc Gemita 1g mà ungthutap.com đã tổng hợp từ các nguồn sau:
- Tờ hướng dẫn sử dụng đi kèm khi mua thuốc.
- Dược thư Quốc Gia Việt Nam mới nhất như: Drugbank, Thuốc biệt dược,Pharmog, Điều trị,…
- Nguồn thông tin y khoa uy tín trên thế giới: Drugs, WebMD, NIH,…
- Nội dung được sàng lọc kỹ lưỡng và trình bày một cách dễ hiểu nhất để bạn nắm bắt thông tin và sử dụng thuốc được dễ dàng, hiệu quả.
- Nội dung không thay thế tờ hướng dẫn sử dụng thuốc và lời khuyên từ bác sĩ. Chúng tôi không đưa ra các lời khuyên và khuyến nghị nào cho việc dùng thuốc!
Sản phẩm tương tự
Giá thuốc Gemita 1g là bao nhiêu?
- Gemita 1g hiện đang được bán sỉ lẻ tại Trường Anh Pharm. Các bạn vui lòng liên hệ hotline công ty Call/Zalo: 090.179.6388 để được giải đáp thắc mắc về giá.
Mua thuốc Gemita 1g ở đâu?
Các bạn có thể dễ dàng mua Gemita 1g tại Trường Anh Pharm bằng cách
- Mua hàng trực tiếp tại cửa hàng (Liên hệ trước khi tới để kiểm tra còn hàng hay không)
- Mua hàng trên website : https://ungthutap.com
- Mua hàng qua số điện thoại hotline : Call/Zalo: 090.179.6388 để được gặp dược sĩ đại học tư vấn cụ thể và nhanh nhất.
Câu hỏi thường gặp
Ung thư TAP hiện nay là một trong những website bán Gemita 1g - Thuốc trị ung thư kết hợp hiệu quả của Ấn Độ chính hãng mà quý khách hàng có thể tin tưởng và đặt mua hàng. Để mua hàng tại Ung thư TAP, bạn có thể lựa chọn một trong các cách thức như sau:
- Mua hàng trực tiếp tại cửa hàng theo khung giờ sáng:9h-11h30, chiều: 2h-4h.
- Đặt hàng và mua trên website : https://ungthutap.com
- Gọi điện qua số điện thoại Hotline 0971.899.466 hoặc nhắn tin qua Zalo: 090.179.6388 để được gặp dược sĩ đại học tư vấn cụ thể và nhanh nhất.
Tuyên bố miễn trừ trách nhiệm:
Tất cả các thông tin được cung cấp trên trang web này chỉ là những thông tin tổng quan, không được xem là tư vấn y khoa và không nhằm mục đích thay thế cho việc tư vấn, chẩn đoán từ bác sĩ hay các chuyên viên y tế. Chúng tôi luôn nỗ lực để có thể cập nhật những thông tin mới và chính xác đến người đọc. Đồng thời, chúng tôi cũng không tuyên bố hay bảo đảm dưới bất kỳ hình thức nào, rõ ràng hay ngụ ý, về tính chất đầy đủ, chính xác, kịp thời, đáng tin cậy, phù hợp hoặc sẵn có với những thông tin, sản phẩm, dịch vụ hoặc hình ảnh, hay các thông tin trong văn bản có liên quan và tất cả các tài liệu khác có trên website cho bất kỳ mục đích nào. Chính vì vậy, bạn đọc không thể áp dụng cho bất kỳ tình trạng y tế của cá nhân nào và có thể sẽ xảy ra rủi ro cho người đọc khi dựa vào những thông tin đó.
Sản phẩm liên quan
Sản phẩm cùng hãng
Bình luận
Bạn hãy là người đầu tiên nhận xét về sản phẩm này