Mevarex 50mg - Thuốc điều trị ung thư phổi tế bào nhỏ hiệu quả
Liên hệ
Chính sách khuyến mãi
Dược sỹ tư vấn 24/7.
Khách hàng lấy sỉ, sll vui lòng liên hệ call/Zalo để được cập nhật giá
Sản phẩm chính hãng, cam kết chất lượng.
Kiểm tra hàng trước khi thanh toán.
Vận chuyển toàn quốc: 25.000đ/đơn (< 2kg)
Thông tin dược phẩm
Nhà sản xuất:
Số đăng ký:
QLĐB-640-17
Hoạt chất:
Hoạt chất/Hàm lượng:
Etoposid - 50 mg
Hạn sử dụng:
24 tháng.
Công ty đăng ký:
Công ty cổ phần SPM.
Video
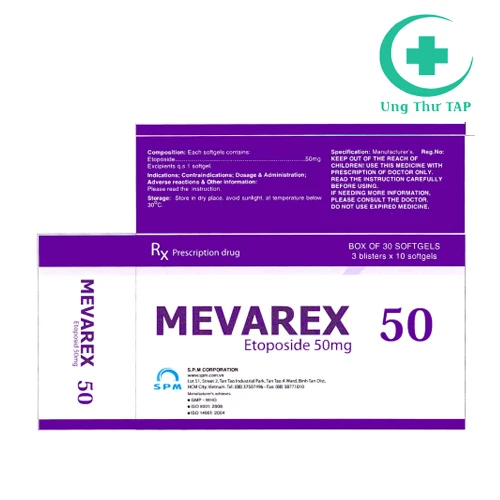
Mevarex 50 là thuốc gì?
- Mevarex 50 là một loại thuốc chống ung thư, có thể dùng riêng lẻ hoặc kết hợp với các thuốc tiêu u khác trong việc điều trị ung thư phổi tế bào nhỏ và ung thư biểu bì tinh hoàn kháng trị đã qua phẫu thuật. Dưới đây, Ungthutap.com sẽ cung cấp các thông tin chi tiết nhất về công dụng, chỉ định của thuốc, liệu dùng & cách dùng cụ thể cùng với một số thông tin liên quan khác về thuốc.
Dạng bào chế
- Viên nang mềm.
Quy cách đóng gói
- Hộp 3 vỉ x 10 viên.
Thành phần – Nồng độ/hàm lượng
- Etoposid - 50 mg.
Thông tin về hoạt chất
- Dược lý học:
- Etoposid có tác dụng làm ngừng giai đoạn trung kỳ trên nguyên bào sợi của gà con, nhưng tác dụng chính của nó ở các tế bào động vật có vú là ở giai đoạn G2. Có 2 đáp ứng khác nhau tùy theo liều. Ở nồng độ cao (≥ 10 µg/ml) in vitro, các tế bào tham gia quá trình phân bào bị phân giải. Ở nồng độ thấp (0,3 – 10 µg/ml) các tế bào bị ức chế ở giai đoạn tiền kỳ. Thuốc không ức chế tập hợp sợi thoi. Tác dụng chủ yếu của etoposid ở mức đại phân tử là làm gẫy chuỗi DNA do tương tác với DNA topoisomerase II hoặc tạo thành các gốc tự do.
- Dược động học:
- Thuốc được phân bố nhanh qua đường truyền tĩnh mạch và nồng độ trong huyết tương giảm theo 2 pha với nửa đời phân bố khoảng 1,5 giờ và nửa đời thải trừ cuối cùng là 3 – 19 giờ. Thể tích phân bố trung bình ở giai đoạn ổn định giảm xuống từ 18 – 29 lít hay từ 7 – 17 lít/m2 ở người lớn và 5 – 10 lít/m2 ở trẻ em. Thuốc qua hàng rào máu – não rất ít với nồng độ ở dịch não tủy bằng 1 – 10% nồng độ thuốc trong huyết tương. Nồng độ thuốc trong phổi bình thường cao hơn trong trường hợp phổi bị di căn và tại khối u nguyên phát bằng tại mô bình thường của cơ tử cung. Thuốc liên kết chặt chẽ với protein huyết tương, khoảng 94 – 97% in vitro và được chuyển hoá ở gan thành dẫn chất hydroxy acid và cislacton. Etoposid bài xuất theo nước tiểu và phân dưới dạng nguyên vẹn và các chất chuyển hóa. Khoảng 45% lượng thuốc được bài xuất qua nước tiểu trong 72 giờ, trong đó 2/3 ở dạng không biến đổi; 16% lượng thuốc được bài tiết theo phân và 6% hoặc ít hơn được bài tiết qua mật
Tác dụng - Chỉ định của thuốc Mevarex 50
- MEVAREX là một thuốc chống ung thư dùng đường uống, có thể được dùng riêng lẻ hoặc kết hợp với các thuốc tiêu u khác.
- Dữ liệu hiện tại cho thấy rằng MEVAREX được dùng để điều trị ung thư phổi tế bào nhỏ, ung thư biểu bì tinh hoàn kháng trị đã qua phẫu thuật
Chống chỉ định của thuốc Mevarex 50
- Không dùng cho những người bệnh bị quá mẫn từ trước với etoposid hay bất kỳ thành phần nào có trong thuốc.
- MEVAREX chống chỉ định ở các bệnh nhân bị suy gan nặng
- Dùng đồng thời với vaccin sốt vàng hoặc các vaccin sống khác bị chống chỉ định ở các bệnh nhân bị ức chế miễn dịch
Liều lượng - Cách dùng của thuốc Mevarex 50
- Cách dùng:
- Dùng uống. Thuốc nên uống lúc đói.
- Liều dùng:
- Liều khuyến cáo của MEVAREX là 120-240 mg/m2 uống hàng ngày, trong 5 ngày liên tiếp. Liều hàng ngày cao hơn 200 mg nên được chia làm 2 lần (BID). Sinh khả dụng cũng khác nhau giữa các bệnh nhân sau bất kỳ liều uống nào. Điều này nên được xem xét khi kê đơn thuốc này. Trong việc xem xét sự khác nhau đáng kể giữa các bệnh nhận, cần điều chỉnh liều để đạt được hiệu quả điều trị mong muốn. Vì MEVAREX gây ức chế tủy xương, các liều không được lặp lại thường xuyên hơn ở các khoảng thời gian 21 ngày. Trong bất kỳ trường hợp nào, liều lặp lại của MEVAREX không được cung cấp đến khi công thức máu được kiểm tra về bằng chứng ức chế tủy xương và được thấy thỏa đáng
- Điều chỉnh liều:
- Liều của MEVAREX nên được điều chỉnh theo hiệu quả ức chế tủy xương của các thuốc khác kết hợp hoặc hiệu quả trước khi điều trị tia X hoặc hóa trị vì chúng làm tổn thương phần tủy xương còn lại.
- Các bệnh nhân không nên bắt đầu chu kỳ điều trị mới bằng MEVAREX nếu số lượng bạch cầu trung tính dưới 1.500 tế bào/mm3 hoặc số lượng tiểu cầu dưới 100,000 tế bào/mm3, trừ phi gây bởi bệnh ác tính.
- Liều tiếp sau liều ban đầu nên được điều chỉnh nếu số lượng bạch cầu trung tính dưới 500 tế bào/mm3 xảy ra trên 5 ngày hoặc liên quan đến sốt hoặc nhiễm trùng, nếu số lượng tiểu cầu dưới 25.000 tế bào/mm3 xảy ra, nếu bất ký độc tính cấp 3 hoặc 4 phát triển hoặc độ thanh thải của thận dưới 50 ml/phút
- Người cao tuổi: Không cần điều chỉnh liều.
- Trẻ em: Độ an toàn và hiệu quả ở trẻ em chưa được xác lập.
- Suy thận:
- Ở các bệnh nhân có chức năng thận bị suy, điều chỉnh liều sau liều ban đầu nên được xem xét dựa trên độ thanh thải creatinln đo được.
- Độ thanh thải creatinin đo được > 50 ml/phút 100% liều của etoposid
- Độ thanh thải creatinin đo được 15 – 50 ml/phút 75% liều của etoposid
- Liều sau nên dựa trên sự dung nạp cùa bệnh nhân và hiệu quả lâm sàng. Dữ liệu không có sẵn ở các bệnh nhân có độ thanh thải Creatinin <15 mL/phút và nên xem xét giảm liều hơn nữa ở các bệnh nhân này.
- Ở các bệnh nhân có chức năng thận bị suy, điều chỉnh liều sau liều ban đầu nên được xem xét dựa trên độ thanh thải creatinln đo được.
Lưu ý đặc biệt, cảnh báo và thận trọng
- MEVAREX nên được dùng bởi những người có kinh nghiệm trong việc sử dụng liệu pháp kháng u
- Ức chế tủy xương nặng với kết quả nhiễm trùng hoặc chảy máu xảy ra
- Ức chế tủy xương tử vong đã được báo cáo sau khi dùng etoposid. Các bệnh nhân được điều trị bằng MEVAREX phải được quan sát ức chế tủy xương cẩn thận và thường xuyên cả trong và sau điều trị. ức chế tủy xương giới hạn liều là độc tính đáng kể nhất liên quan đến điều trị bằng MEVAREX. Các nghiên cứu sau có được lúc bắt đầu điều trị và trước mỗi liều tiếp theo của MEVAREX: số lượng tiểu cầu, hemoglobin, số lượng bạch cầu và sự khác nhau.
- Nếu xạ trị và/hoặc hóa trị được thực hiện trước khi bắt đầu điều trị bằng MEVAREX, một khoảng phù hợp cho phép khả năng tủy xựơng phục hồi. Nếu số lượng bạch cầu giảm dưới 2.000mm , việc điều trị tạm ngừng đến khi các yếu tố của máu tuân hoàn trở lại các mức chấp nhận (tiểu cầu trên 100.000 mm3, bạch cầu trên 4.000/mm3), điều này thường trong 10 ngày.
- MEVAREX không được sử dụng ở các bệnh nhân có số lượng bạch cầu trung tính dưới 1.500 tế bào/mm3 hoặc số lượng tiểu cầu dưới 100.000 tế bào/mm3, trừ phi gây bởi bệnh ác tính.
- Liều tiếp theo liều ban đầu nên được điều chỉnh nếu số lượng bạch cầu trụng tính dưới 500 tế bào/mm3 xảy ra trên 5 ngày hoặc liên quan đến sốt hoặc nhiễm trùng, nếu số lượng tiểu cầu dưới 25.000 tế bào/mm3 xảy ra, nếu độc tính cấp 3 hoặc 4 phát triển hoặc nếu độ thanh thải thận dưới 50 ml/phút. Liều nên được điều chỉnh theo hiệu quả ức chế tủy xương của các thuốc khác kết hợp hoặc hiệu quả trước khi điều trị tia X hoặc hóa trị vì chúng làm tổn thương phần tủy xương còn lại.
- Các bệnh nhân có albumin huyết thanh thấp có thể tăng nguy cơ độc tính liên quan etoposid. Số lượng máu ngoại biên và chức năng gan nên được theo dõi. Các bệnh nhân có chức năng gan và thận bị suy giảm cần theo dõi chức năng gan và thận do nguy cơ tích lũy.
- Nhiễm trùng nên được kiểm soát trước khi điều trị bằng MEVAREX bắt đầu.
- Do khả năng gây đột biến của etoposid, một sự ngừa thai hiệu quả được yêu cầu cho cả bệnh nhân nam và bệnh nhân nữ trong quá trình điều trị và đến 6 tháng sau khi kết thúc điều trị. Cần tư vấn di truyền nếu bệnh nnân ước muốn có con sau khi kết thúc điều trị. Vì etoposid có thể làm giảm khả năng sinh sản của nam giới, bảo quản tinh trùng có thể được xem xét vì mục đích làm cha về sau.
- Xảy ra bệnh bạch cầu cấp, có thể xảy ra có hay không có giai đoạn tiền bệnh bạch cầu đã được báo cáo là hiếm ở các bệnh nhân được điều trị bằng etoposid liên quan đên các thuốc kháng u khác.
- Không có nguy cơ tích lũy, không có các yếu tố ảnh hưởng liên quan đến sự phát triển bệnh bạch cầu thứ phát được biết. Vai trò của cả việc sử dụng thời biểu và liều tích lũy của etoposid được đề nghị, nhưng chưa được xác định rõ.
- Bất thường nhiễm sắc thể 11q23 đã được quan sát ở một số trường hợp bệnh bạch cầu thứ phát ở các bệnh nhân dùng epipodophyllotoxin. Bất thường này cũng được thấy ở các bệnh nhân phát triển bệnh bạch cầu thứ phát sau khi được điều trị bằng chế độ hóa trị không chứa epipodophyllotoxin và trong bệnh bạch cầu xảy ra lần nữa. Đặc tính khác liên quan đến bệnh bạch cầu thứ phát ở các bệnh nhân dùng epipodophyllotoxin xuất hiện thời kỳ ủ bệnh ngắn, với thời gian trung bình phát triển bệnh bạch cầu là khoảng 32 tháng
- Trong tất cả các trường hợp, việc sử dụng MEVAREX được xem là hóa trị, thầy thuốc phải đánh giá nhu cầu và sự có ích của thuốc ngược với nguy cơ các phản ứng có hại. Hầu hết các phản ứng có hại là phục hồi nếu được phát hiện sớm. Nếu các phản ứng nghiêm trọng xảy ra, nên giảm liều hoặc ngừng và thực hiện các biện pháp khắc phục thích hợp theo đánh giá lâm sàng của thầy thụốc. Tái điều trị bằng MEVAREX nên được thực hiện thận trọng và xem xét đầy đủ nhu cầu thêm về thuốc và thật chú ý đến khả năng tái phát độc tính.
- Hội chứng tiêu u (đôi khi tử vong) đã được báo cáo sau khi sử dụng etoposid cùng với các thuốc hóa trị khác, cần theo dõi chặt chẽ bệnh nhân để phát hiện các dấu hiệu sớm về hội chứng tiêu u, đặc biệt ở các bệnh nhân có các yếu tố nguy cơ như các khối u lớn nhạy cảm điều trị, và suy thận. Các biện pháp phòng ngừa thích hợp cần được xem xét ở các bệnh nhân có nguy cơ về biến chứng điều trị này.
- Propyl paraben (nipasol) ảnh hường đến cơ quan sinh sản của giống đực, thận trọng khi dùng cho nam giới.
- Sản phẩm chứa glycerin có thể gây đau đầu.
- Sản phẩm chứa sorbitol, các bệnh nhân có vấn đề di truyền hiếm về không dung nạp fructose không được dùng sản phẩm này.
- Sản phẩm có chứa màu vàng tartrazin có thể gây phản ứng dị ứng
Sử dụng cho phụ nữ có thai hoặc đang cho con bú
- Thời kỳ mang thai:
- MEVAREX có thể gây hại bào thai khi được dùng cho phụ nữ mang thai. Etoposid là tác nhân gây quái thai ở chuột cống và chuột nhắc ở các mức liều tương đương các liều thử lâm sàng. Không có các nghiên cứu đủ và được kiểm soát tốt ở phụ nữ mang thai.
- MEVAREX thường không được dùng cho phụ nữ có thai hoặc phụ nữ đang cho con bú. Những phụ nữ có khả năng có thai được tư vấn tránh có thai.
- Nếu thuốc này được sử dụng trong quá trình mang thai, hoặc nếu bệnh nhân có thai trong khi dùng thuốc này, bệnh nhân cần được thông báo về khả năng có hại cho bào thai.
- Do khả năng gây đột biến của etoposid, sự ngừa thai hiệu quả được yêu cầu cho cả bệnh nhân nam và nữ trong quá trình điều trị và đến 6 tháng sau khi kết thúc điều trị. cần tư vấn di truyền nếu bệnh nhân ước muốn có con sau khi kết thúc điều trị. Vì etoposid có thể làm giảm khả năng sinh sản của nam giới, bảo quản tinh trùng có thể được xem xét vì mục đích làm cha về sau.
- Ảnh hưởng của MEVAREX đến sự sinh sản ở người chưa được xác định.
- Các thử nghiệm In-vitro cho thấy rằng MEVAREX gây đột biến
- Thời kỳ cho con bú:
- Không biết thuốc này có được bài tiết vào sữa người không. Bởi vì tiết vào sữa người và bởi khả năng các phản ứng có hại nặng ở trẻ l một quyết định được đưa ra hoặc ngừng cho con bú hoặc ngừng thuố của thuốc đối với người mẹ
Sử dụng cho người lái xe và vận hành máy móc
- Không có nghiên cứu về ảnh hưởng của etoposid khi lái xe và vận hành máy móc. Nếu bệnh nhân có những tác dụng phụ như mệt mỏi, buồn ngủ thì nên tránh lái xe và vận hành máy móc.
Tác dụng phụ của thuốc Mevarex 50
- Huyết hoc:
- ức chế tủy xương với hậu quả tử vong đã được báo cáo sau khi dùng etoposid.
- ức chế tủy xương là độc tính giới hạn liều thường xuyên nhất. Sự phục hồi của tủy xương thường hoàn tất trong 20 ngày, và không có độc tính tích lũy được báo cáo.
- Số lượng bạch cầu hạt và tiểu cầu thấp có khuynh hướng xảy ra vào khoảng 10-14 ngày sau khi dùng etoposid hoặc etoposid phosphat tùy thuộc vào cách dùng và thời gian điều trị. Số lượng thấp có khuynh hướng xảy ra sớm hơn với việc dùng tiêm tĩnh mạch được so sánh với dùng đường uống. Giảm bạch cầu và giảm bạch cậu nặng (dưới 1.000 tê bào/mm3) được quan sát ở 60% đến 91% và 7% đến 17%, lần lượt, bệnh nhân được điều trị bằng MEVAREX đơn trị. Giảm tiểu cầu và giảm tiểu cầu nặng (dưới 50.000 tiểu cầu/mm3) được quan sát ở 28% đến 41% và 4% đến 20 %, lần lượt, của cùng nhóm bênh nhân này
- Các báo cáo về sốt và nhiễm trùng cũng rất thường xuyên ở các bệnh nhân có bạch cầu trung tính được điều trị bằng etoposid/etoposid phosphat. Thiếu máu xảy ra không thường xuyên.
- Số lượng bạch cầu thấp xảy ra khoảng 21 ngày sau khi điều trị. Rung tóc:
- Rụng tóc phục hồi, đôi khi tiến triển thành rụng tóc toàn bộ, được quan sát ở đến 66% bệnh nhân.
- Tiêu hóa:
- Buồn nôn và nôn là các nhiễm độc tiêu hóa chính và xảy ra ở trên 1/3 số bệnh nhân.
- Chống nôn là hữu ích trong việc kiểm soát các tác dụng phụ này. Đau bụng, chán ăn, tiêu chảy, viêm thực quản và viêm dạ dày xảy ra không thường xuyên.
- Thay đổi huyết áp
- Tăng huyết áp:
- Trong các nghiên cứu lâm sàng liên quan đến etoposid, các triệu chứng tăng huyết áp đã được báo cáo. Nếu tăng huyết áp đáng kể về lâm sàng xảy ra ở các bệnh nhân dùng MEVAREX, phải bắt đầu điều trị hổ trợ thích hợp.
- Các phản ứng dị ứng:
- Các phản ứng mẫn cảm cũng được báo cáo xảy ra trong hoặc ngay sau khi tiêm tĩnh mạch etoposid. Nồng độ hay tốc độ truyền giữ vai trò như thế nào trong phát triển các phản ứng mẫn cảm là không chắc chắn. Huyết áp thường trở lại bình thường trong vài giờ sau khi ngừng truyền. Các phản ứng mẫn cảm có thể xảy ra ở liều ban đầu của MEVAREX.
- Các phản ứng tử vong cấp liên quan đến co thắt phế quản đã được báo cáo với MEVAREX.
- MEVAREX cho thấy đạt nồng độ cao trong gan và thận, vì vậy cho thấy khả năng tích lũy trong các trường hợp suy chức năng.
- Các biến chứng chuyển hóa
- Hội chứng tiêu u (đôi khi tử vong) được báo cáo sau khi dùng MEVAREX liên quan đến các thuốc hóa trị khác
Tương tác thuốc
- Dùng đồng thời etoposid đường uống với cyclosporin liều cao (dẫn đến nồng độ trên 2000 ng/ml) dẫn đến tăng 80% lượng etoposid (AUC). Độ thanh thải toàn phần của etoposid giảm 38% được so sánh với etoposid đơn lẻ.
- Điều trị đồng thời cisplatin liên quan đến giảm độ thanh thải toàn phần của etoposid.
- Điều trị đồng thời phenytoin liên quan đến tăng độ thanh thải etoposid và giảm hiệu quả.
- Điều trị đồng thời warfarin có thể kéo dài thời gian đông máu (INR). cần theo dõi chặt chẽ INR.
- Có nguy cơ bệnh tiêm chủng hệ thống tử vong tăng với việc sử dụng vaccin sốt vàng. Các vaccin sống bị chống chỉ định ở các bệnh nhân bị ức chế miễn dịch.
- Sử dụng trước hoặc đồng thời các thuốc khác có tác dụng ức chế tủy xương tương tự etoposid/etoposid phosphat có thể có các tác dụng cộng gộp hay hiệp lực.
- In vitro về liên kết protein huyết tương là 97%. Phenylbutazon, natri salicylat, và aspirin có thể đổi chỗ etoposid trong liên kết protein huyết tương.
- Kháng chéo giữa anthracyclin và etoposid được báo cáo trong các thí nghiệm tiền lâm sàng.
Quá liều và xử trí
- Không có thuốc giải độc đã được chứng minh được thiết lập cho quá liều etoposid. Điều trị triệu chứng và hỗ trợ.
- Liều tổng 2,4 – 3,5 g/m2 dùng đường i.v. trên 3 ngày gây viêm màng nhầy và nhiễm độc tủy. Nhiễm acid chuyển hóa và các trường hợp nhiễm độc gan nặng được báo cáo ở các bệnh nhân dùng liều etoposid cao hơn liều được khuyến cáo.
Bảo quản
- Bảo quản ở nhiệt độ không quá 30°C. Tránh ánh sáng. Để xa tầm tay của trẻ em.
Hạn sử dụng
- 24 tháng.
Nhà sản xuất
- Công ty cổ phần SPM.
Sản phẩm tương tự
Giá thuốc Mevarex 50 là bao nhiêu?
- Mevarex 50 hiện đang được bán sỉ lẻ tại Trường Anh Pharm. Các bạn vui lòng liên hệ hotline công ty Call/Zalo: 090.179.6388 để được giải đáp thắc mắc về giá.
Mua thuốc Mevarex 50 ở đâu?
Các bạn có thể dễ dàng mua Mevarex 50 tại Trường Anh Pharm bằng cách
- Mua hàng trực tiếp tại cửa hàng (Liên hệ trước khi tới để kiểm tra còn hàng hay không)
- Mua hàng trên website : https://ungthutap.com
- Mua hàng qua số điện thoại hotline : Call/Zalo: 090.179.6388 để được gặp dược sĩ đại học tư vấn cụ thể và nhanh nhất.
Câu hỏi thường gặp
Ung thư TAP hiện nay là một trong những website bán Mevarex 50mg - Thuốc điều trị ung thư phổi tế bào nhỏ hiệu quả chính hãng mà quý khách hàng có thể tin tưởng và đặt mua hàng. Để mua hàng tại Ung thư TAP, bạn có thể lựa chọn một trong các cách thức như sau:
- Mua hàng trực tiếp tại cửa hàng theo khung giờ sáng:9h-11h30, chiều: 2h-4h.
- Đặt hàng và mua trên website : https://ungthutap.com
- Gọi điện qua số điện thoại Hotline 0971.899.466 hoặc nhắn tin qua Zalo: 090.179.6388 để được gặp dược sĩ đại học tư vấn cụ thể và nhanh nhất.
Tuyên bố miễn trừ trách nhiệm:
Tất cả các thông tin được cung cấp trên trang web này chỉ là những thông tin tổng quan, không được xem là tư vấn y khoa và không nhằm mục đích thay thế cho việc tư vấn, chẩn đoán từ bác sĩ hay các chuyên viên y tế. Chúng tôi luôn nỗ lực để có thể cập nhật những thông tin mới và chính xác đến người đọc. Đồng thời, chúng tôi cũng không tuyên bố hay bảo đảm dưới bất kỳ hình thức nào, rõ ràng hay ngụ ý, về tính chất đầy đủ, chính xác, kịp thời, đáng tin cậy, phù hợp hoặc sẵn có với những thông tin, sản phẩm, dịch vụ hoặc hình ảnh, hay các thông tin trong văn bản có liên quan và tất cả các tài liệu khác có trên website cho bất kỳ mục đích nào. Chính vì vậy, bạn đọc không thể áp dụng cho bất kỳ tình trạng y tế của cá nhân nào và có thể sẽ xảy ra rủi ro cho người đọc khi dựa vào những thông tin đó.
Sản phẩm liên quan
Sản phẩm cùng hãng
Bình luận
Bạn hãy là người đầu tiên nhận xét về sản phẩm này