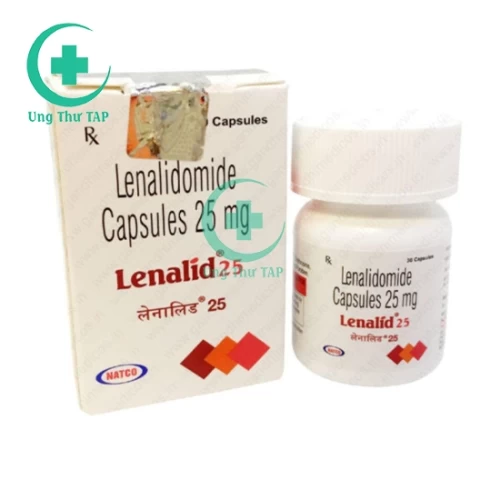
Lenalid 25 (Lenalidomide 25mg) - Thuốc trị đa u tủy hiệu quả
Liên hệ
Chính sách khuyến mãi
Dược sỹ tư vấn 24/7.
Khách hàng lấy sỉ, sll vui lòng liên hệ call/Zalo để được cập nhật giá
Sản phẩm chính hãng, cam kết chất lượng.
Kiểm tra hàng trước khi thanh toán.
Vận chuyển toàn quốc: 25.000đ/đơn (< 2kg)
Thông tin dược phẩm
Nhà sản xuất:
Số đăng ký:
Chưa cập nhật
Hoạt chất:
Hoạt chất/Hàm lượng:
Lenalidomide 25mg -
Hạn sử dụng:
24 tháng
Công ty đăng ký:
Natco Pharma
Xuất xứ:
Ấn Độ
Đóng gói:
Hộp 1 lọ 30 viên
Dạng bào chế:
Viên nén
Video
Lenalid 25mg là thuốc gì?
- Lenalid 25mg được chỉ định để điều trị ở những người bị đa u tủy khi sử dụng kết hợp cùng với dexamethasone. Lenalid 25mg còn điều trị hội chứng thần kinh đệm, và sử dụng trong hỗ trợ giải phẫu hạch bạch huyết. Ngoài ra, thuốc còn được chỉ định sử dụng để điều trị bệnh nhân người lớn mắc bệnh u lympho tế bào lớp vỏ tái phát hoặc khó chữa dưới dạng đơn trị liệu. Dưới đây. Ungthutap.com sẽ cung cấp các thông tin chi tiết nhất về công dụng, chỉ định của thuốc, liệu dùng & cách dùng cụ thể cùng với một số thông tin liên quan khác về thuốc.
Thông tin thuốc Lenalid 25mg
- Nhóm thuốc: Thuốc ức chế miễn dịch khác.
- Hoạt chất chính: Lenalidomide.
- Hàm lượng: 25mg.
- Dạng bào chế: Viên nén.
- Quy cách đóng gói: Hộp 30 viên nén.
- Xuất xứ: Ấn Độ.
Đặc tính dược lý của thuốc
- Dược lực học:
- Lenalidomide liên kết trực tiếp với cereblon, một thành phần của phức hợp enzyme ligase E3 ubiquitin vòng cullin bao gồm protein liên kết gây tổn thương axit deoxyribonucleic (DNA) 1 (DDB1), cullin 4 (CUL4), và chất điều hòa cullin 1 (Roc1). Trong các tế bào tạo máu, lenalidomide liên kết với cereblon thu nạp các protein cơ chất Aiolos và Ikaros, các yếu tố phiên mã lymphoid, dẫn đến sự biến đổi ở khắp nơi của chúng và sự suy thoái sau đó dẫn đến tác dụng gây độc tế bào và điều hòa miễn dịch trực tiếp.
- Cụ thể, lenalidomide ức chế sự tăng sinh và tăng cường quá trình apoptosis của một số tế bào khối u tạo máu (bao gồm tế bào khối u huyết tương MM, tế bào khối u lympho nang và những tế bào bị mất đoạn nhiễm sắc thể 5), tăng cường miễn dịch qua trung gian tế bào T cell- và Natural Killer (NK) và tăng số lượng tế bào NK, T và NK T. Trong MDS Del (5q), lenalidomide ức chế chọn lọc dòng nhân bản bất thường bằng cách tăng quá trình chết rụng của tế bào Del (5q).
- Sự kết hợp của lenalidomide và rituximab làm tăng ADCC và quá trình apoptosis trực tiếp của khối u trong các tế bào u lympho nang.
- Cơ chế hoạt động của lenalidomide cũng bao gồm các hoạt động bổ sung như đặc tính chống tạo mạch và tạo hồng cầu. Lenalidomide ức chế sự hình thành mạch bằng cách ngăn chặn sự di chuyển và kết dính của các tế bào nội mô và sự hình thành các vi mạch, tăng cường sản xuất hemoglobin của thai nhi bởi các tế bào gốc tạo máu CD34 +, và ức chế sản xuất các cytokine gây viêm (ví dụ, TNF-α và IL-6) bởi bạch cầu đơn nhân.
- Dược động học:
- Sự hấp thụ:
- Lenalidomide được hấp thu nhanh chóng sau khi uống ở những người tình nguyện khỏe mạnh, trong điều kiện đói, với nồng độ tối đa trong huyết tương xảy ra trong khoảng từ 0,5 đến 2 giờ sau khi dùng liều. Ở bệnh nhân, cũng như ở những người tình nguyện khỏe mạnh, nồng độ tối đa (C max ) và đường cong thời gian theo diện tích dưới nồng độ (AUC) tăng tỷ lệ thuận với việc tăng liều. Nhiều liều lượng không gây ra sự tích tụ thuốc rõ rệt. Trong huyết tương, sự phơi nhiễm tương đối của các đồng phân đối quang S và R của lenalidomide lần lượt là khoảng 56% và 44%.
- Sử dụng đồng thời với một bữa ăn giàu chất béo và calo cao ở những người tình nguyện khỏe mạnh làm giảm mức độ hấp thu, dẫn đến giảm khoảng 20% diện tích dưới nồng độ so với đường cong thời gian (AUC) và giảm 50% C max trong huyết tương. Tuy nhiên, trong các thử nghiệm đăng ký hội chứng đa u tủy và u tủy xương chính, nơi tính hiệu quả và an toàn được thiết lập đối với lenalidomide, sản phẩm thuốc được sử dụng mà không liên quan đến lượng thức ăn. Do đó, lenalidomide có thể được sử dụng cùng với thức ăn hoặc không.
- Các phân tích dược động học dân số chỉ ra rằng tỷ lệ hấp thu lenalidomide qua đường uống là tương tự ở bệnh nhân MM, MDS và MCL.
- Phân phối
- In vitro ( 14 C) -lenalidomide gắn kết với protein huyết tương thấp với liên kết trung bình với protein huyết tương lần lượt là 23% và 29% ở bệnh nhân đa u tủy và người tình nguyện khỏe mạnh.
- Lenalidomide có trong tinh dịch của người (<0,01% liều dùng) sau khi dùng 25 mg / ngày và sản phẩm thuốc không thể phát hiện được trong tinh dịch của một đối tượng khỏe mạnh 3 ngày sau khi ngừng sử dụng chất này (xem phần 4.4).
- Biến đổi sinh học và loại bỏ
- Kết quả từ các nghiên cứu chuyển hóa trong ống nghiệm ở người chỉ ra rằng lenalidomide không bị chuyển hóa bởi enzym cytochrom P450 cho thấy rằng việc sử dụng lenalidomide với các sản phẩm thuốc ức chế enzym cytochrom P450 không có khả năng dẫn đến tương tác chuyển hóa thuốc ở người. Các nghiên cứu in vitro chỉ ra rằng lenalidomide không có tác dụng ức chế CYP1A2, CYP2C9, CYP2C19, CYP2D6, CYP2E1, CYP3A hoặc UGT1A1. Do đó, lenalidomide không có khả năng gây ra bất kỳ tương tác thuốc nào có liên quan về mặt lâm sàng khi dùng đồng thời với các chất nền của các enzym này.
- Các nghiên cứu in vitro chỉ ra rằng lenalidomide không phải là chất nền của protein kháng ung thư vú ở người (BCRP), chất vận chuyển protein đa kháng (MRP) MRP1, MRP2 hoặc MRP3, chất vận chuyển anion hữu cơ (OAT) OAT1 và OAT3, polypeptide vận chuyển anion hữu cơ 1B1 ( OATP1B1), chất vận chuyển cation hữu cơ (OCT) OCT1 và OCT2, protein đùn đa chất và độc tố (MATE) MATE1, và tiểu thuyết chất vận chuyển cation hữu cơ (OCTN) OCTN1 và OCTN2.
- Các nghiên cứu in vitro chỉ ra rằng lenalidomide không có tác dụng ức chế bơm xuất muối mật của con người (BSEP), BCRP, MRP2, OAT1, OAT3, OATP1B1, OATP1B3 và OCT2.
- Phần lớn lenalidomide được thải trừ qua đường bài tiết nước tiểu. Sự đóng góp của bài tiết qua thận vào tổng độ thanh thải ở những người có chức năng thận bình thường là 90%, với 4% lenalidomide được thải trừ qua phân.
- Lenalidomide chuyển hóa kém vì 82% liều dùng được bài tiết dưới dạng không đổi qua nước tiểu. Hydroxy-lenalidomide và N-acetyl-lenalidomide tương ứng chiếm 4,59% và 1,83% liều bài tiết. Sự thanh thải lenalidomide ở thận vượt quá mức lọc cầu thận và do đó ít nhất được tiết tích cực ở một mức độ nào đó.
- Ở liều 5 đến 25 mg / ngày, thời gian bán hủy trong huyết tương khoảng 3 giờ ở người tình nguyện khỏe mạnh và từ 3 đến 5 giờ ở bệnh nhân đa u tủy, hội chứng rối loạn sinh tủy hoặc u lympho tế bào lớp vỏ.
Tác dụng - Chỉ định của thuốc Lenalid 25mg
- Bệnh đa u tủy
- Lenalid dưới dạng đơn trị liệu được chỉ định để điều trị duy trì cho bệnh nhân người lớn mắc bệnh đa u tủy xương mới được chẩn đoán đã trải qua phương pháp cấy ghép tế bào gốc tự thân.
- Lenalid dưới dạng liệu pháp kết hợp với dexamethasone, hoặc bortezomib và dexamethasone, hoặc melphalan và prednisone được chỉ định để điều trị cho bệnh nhân người lớn bị đa u tủy chưa được điều trị trước đó không đủ điều kiện để cấy ghép.
- Lenalid kết hợp với dexamethasone được chỉ định để điều trị đa u tủy ở bệnh nhân người lớn đã được điều trị ít nhất một lần trước đó.
- Hội chứng thần kinh đệm
- Lenalid dưới dạng đơn trị liệu được chỉ định để điều trị bệnh nhân người lớn bị thiếu máu phụ thuộc vào truyền máu do hội chứng rối loạn sinh tủy có nguy cơ thấp hoặc trung bình liên quan đến bất thường di truyền tế bào 5q mất đoạn cô lập khi các lựa chọn điều trị khác không đủ hoặc không đầy đủ.
- U lympho tế bào áo choàng
- Lenalid dưới dạng đơn trị liệu được chỉ định để điều trị bệnh nhân người lớn mắc bệnh u lympho tế bào lớp vỏ tái phát hoặc khó chữa.
- Giải phẫu hạch bạch huyết
- Lenalid kết hợp với rituximab (kháng thể chống CD20) được chỉ định để điều trị cho bệnh nhân người lớn bị ung thư hạch dạng nang đã được điều trị trước đó.
Chống chỉ định của thuốc Lenalid 25mg
- Không sử dụng cho người mẫn cảm với bất kỳ thành phần nào của thuốc.
- Không dùng cho phụ nữ mang thai, cho con bú và bệnh nhân dưới 18 tuổi.
- Không dùng cho người bị tăng calci huyết (hàm lượng calci tăng bất bình thường trong máu).
- Không dùng cho người bị tăng calci niệu (thải trừ calci quá mức trong nước tiểu).
- Không dùng cho bệnh nhân bị sỏi calci (sỏi thận).
- Không dùng cho bệnh nhân bất động lâu ngày kèm theo tăng calci huyết và/hoặc tăng calci niệu.
Liều lượng - Cách dùng của thuốc Lenalid 25mg
- Cách dùng :
- Uống cả viên lenalid với 1 ly nước đầy, trước hoặc sau bữa ăn
- Mỗi ngày một lần trong 21 ngày và sau đó ngừng 7 ngày. Chu kì điều trị 28 ngày này có thể được lặp lại theo khuyến cáo của bác sĩ.
- Nên uống viên nang thuốc lenalidomide vào cùng một khoảng thời gian mỗi ngày.
- Liều dùng:
- Người lớn mắc bệnh hội chứng loạn sản tủy:
- Liều dùng lenalid 10 mg uống một lần mỗi ngày. Điều trị nên được tiếp tục cho đến khi bệnh tiến triển hoặc độc tính không được chấp nhận.
- Bệnh đa u tủy:
- Liều khởi đầu được đề nghị của Lenalidomine là 25mg uống mỗi ngày một lần vào các ngày 1-21 của chu kỳ 28 ngày lặp lại kết hợp với dexamethasone
- Đối với bệnh nhân > 75 tuổi, có thể giảm liều khởi đầu của dexamethasone. Điều trị nên được tiếp tục cho đến khi bệnh tiến triển hoặc độc tính không được chấp nhận.
- Hội chứng thần kinh đệm:
- Liều khởi đầu được đề nghị của Lenalidomine là 10mg mỗi ngày. Điều trị được tiếp tục hoặc sửa đổi dựa trên kết quả lâm sàng và cận lâm sàng.
- Tế bào lympho tế bào:
- Liều khởi đầu được đề nghị của Lenalidomine là 25mg/ngày uống vào các ngày 1 đến 21 của chu kỳ 28 ngày lặp lại đối với u lympho tế bào lớp vỏ tái phát hoặc chịu lửa.
- Người lớn mắc bệnh hội chứng loạn sản tủy:
Lưu ý đặc biệt, cảnh báo và thận trọng
- Theo dõi chặt chẽ quá trình sử dụng Lenalid để thay đổi liều giảm tác dụng phụ.
- Có thể cần xét nghiệm máu để kiểm tra xem có bất kỳ tác dụng không mong muốn nào không.
- Khám định kì sau khi uống thuốc từ 2-4 tuần tùy theo mức độ nghiêm trọng.
- Giảm bạch cầu trung tính: Gây ra các vấn đề về nhiễm trùng có thể làm giảm khả năng chống nhiễm trùng.
- Giảm tiểu cầu (tiểu cầu cấp): Hãy thận trọng, có thể làm cho những điều kiện tồi tệ hơn.
- Bệnh thận: Nghiêm trọng có thể làm tăng lượng lenalidomide trong cơ thể và tăng nguy cơ tác dụng phụ. Thuốc nên được sử dụng thận trọng ở những bệnh nhân mắc bệnh thận.
- Thuốc nên được sử dụng thận trọng ở những bệnh nhân mắc bệnh gan.
- Nhiều u tủy: Có thể làm tăng nguy cơ mắc tác dụng phụ nghiêm trọng.
Sử dụng cho phụ nữ có thai hoặc đang cho con bú
- Phụ nữ có thai:
- Lenalidomide có liên quan về cấu trúc với thalidomide. Thalidomide là một hoạt chất gây quái thai ở người được biết đến gây ra các dị tật bẩm sinh nghiêm trọng đe dọa tính mạng.
- Lenalidomide gây ra dị tật ở khỉ tương tự như những trường hợp được mô tả với thalidomide. Do đó, lenalidomide có thể gây quái thai và chống chỉ định lenalidomide trong thời kỳ mang thai.
- Phụ nữ đang cho con bú:
- Người ta không biết liệu lenalidomide có bài tiết qua sữa mẹ hay không. Do đó, nên ngừng cho con bú trong thời gian điều trị bằng lenalidomide.
Sử dụng cho người lái xe và vận hành máy móc
- Lenalidomide có ảnh hưởng nhỏ hoặc trung bình đến khả năng lái xe và sử dụng máy móc. Mệt mỏi, chóng mặt, buồn ngủ, chóng mặt và mờ mắt đã được báo cáo khi sử dụng lenalidomide. Do đó, cần thận trọng khi lái xe hoặc vận hành máy móc.
Tác dụng phụ của thuốc Lenalid 25mg
- Đa u tủy mới được chẩn đoán: bệnh nhân đã trải qua ASCT được điều trị bằng duy trì lenalidomide
- Các phản ứng có hại nghiêm trọng được quan sát thấy thường xuyên hơn (≥5%) khi duy trì lenalidomide so với giả dược là:
- Viêm phổi (10,6%; thời kỳ kết hợp) từ IFM 2005-02
- Nhiễm trùng phổi (9,4% [9,4% sau khi bắt đầu điều trị duy trì]) do CALGB 100104
- Trong nghiên cứu IFM 2005-02, các phản ứng có hại được quan sát thấy khi duy trì lenalidomide thường xuyên hơn giả dược là giảm bạch cầu trung tính (60,8%), viêm phế quản (47,4%), tiêu chảy (38,9%), viêm mũi họng (34,8%), co thắt cơ (33,4%) , giảm bạch cầu (31,7%), suy nhược (29,7%), ho (27,3%), giảm tiểu cầu (23,5%), viêm dạ dày ruột (22,5%) và sốt (20,5%).
- Trong nghiên cứu CALGB 100104, các phản ứng có hại được quan sát thấy khi duy trì lenalidomide thường xuyên hơn giả dược là giảm bạch cầu trung tính (79,0% [71,9% sau khi bắt đầu điều trị duy trì]), giảm tiểu cầu (72,3% [61,6%]), tiêu chảy (54,5% [46,4 %]), phát ban (31,7% [25,0%]), nhiễm trùng đường hô hấp trên (26,8% [26,8%]), mệt mỏi (22,8% [17,9%]), giảm bạch cầu (22,8% [18,8%]) và thiếu máu (21,0 % [13,8%]).
- Bệnh nhân đa u tủy mới được chẩn đoán không đủ điều kiện để cấy ghép nhận lenalidomide kết hợp với bortezomib và dexamethasone
- Trong nghiên cứu SWOG S0777, các phản ứng có hại nghiêm trọng được quan sát thấy thường xuyên hơn (≥ 5%) khi dùng lenalidomide kết hợp với bortezomib và dexamethasone tiêm tĩnh mạch so với lenalidomide kết hợp với dexamethasone là:
- Hạ huyết áp (6,5%), nhiễm trùng phổi (5,7%), mất nước (5,0%)
- Các phản ứng ngoại ý được quan sát thấy thường xuyên hơn khi dùng lenalidomide kết hợp với bortezomib và dexamethasone so với lenalidomide kết hợp với dexamethasone là: Mệt mỏi (73,7%), bệnh thần kinh ngoại biên (71,8%), giảm tiểu cầu (57,6%), táo bón (56,1%), hạ canxi máu ( 50.0%).
- Đa u tủy mới được chẩn đoán: bệnh nhân không đủ điều kiện cấy ghép được điều trị bằng lenalidomide kết hợp với dexamethasone liều thấp
- Các phản ứng có hại nghiêm trọng được quan sát thấy thường xuyên hơn (≥5%) khi dùng lenalidomide kết hợp với dexamethasone liều thấp (Rd và Rd18) so với melphalan, prednisone và thalidomide (MPT) là:
- Viêm phổi (9,8%)
- Suy thận (bao gồm cả cấp tính) (6,3%)
- Các phản ứng có hại được quan sát với Rd hoặc Rd18 thường xuyên hơn MPT là: tiêu chảy (45,5%), mệt mỏi (32,8%), đau lưng (32,0%), suy nhược (28,2%), mất ngủ (27,6%), phát ban (24,3%) , giảm cảm giác thèm ăn (23,1%), ho (22,7%), sốt (21,4%) và co thắt cơ (20,5%).
- Đa u tủy mới được chẩn đoán: bệnh nhân không đủ điều kiện cấy ghép được điều trị bằng lenalidomide kết hợp với melphalan và prednisone
- Các phản ứng có hại nghiêm trọng được quan sát thấy thường xuyên hơn (≥5%) với melphalan, prednisone và lenalidomide, sau đó là duy trì lenalidomide (MPR + R) hoặc melphalan, prednisone và lenalidomide sau đó là giả dược (MPR + p) so với melphalan, prednisone và placebo, sau đó là giả dược (MPp + p) là:
- Giảm bạch cầu do sốt (6,0%)
- Thiếu máu (5,3%)
- Các phản ứng ngoại ý quan sát thấy thường xuyên hơn với MPR + R hoặc MPR + p so với MPp + p là: giảm bạch cầu trung tính (83,3%), thiếu máu (70,7%), giảm tiểu cầu (70,0%), giảm bạch cầu (38,8%), táo bón (34,0%), tiêu chảy (33,3%), phát ban (28,9%), sốt (27,0%), phù ngoại vi (25,0%), ho (24,0%), chán ăn (23,7%) và suy nhược (22,0%).
- Đa u tủy: bệnh nhân có ít nhất một lần điều trị trước
- Huyết khối tĩnh mạch
- Giảm bạch cầu cấp độ 4
- Các phản ứng có hại được quan sát xảy ra với lenalidomide và dexamethasone thường xuyên hơn so với giả dược và dexamethasone trong các thử nghiệm lâm sàng đa u tủy (MM-009 và MM-010) là mệt mỏi (43,9%), giảm bạch cầu (42,2%), táo bón (40,5%), tiêu chảy (38,5%), chuột rút (33,4%), thiếu máu (31,4%), giảm tiểu cầu (21,5%), và phát ban (21,2%).
- Hội chứng thần kinh đệm
- Hầu hết các phản ứng phụ có xu hướng xảy ra trong 16 tuần đầu điều trị với lenalidomide.
- Huyết khối tĩnh mạch (huyết khối tĩnh mạch sâu, thuyên tắc phổi)
- Giảm bạch cầu cấp độ 3 hoặc 4, giảm bạch cầu do sốt và giảm tiểu cầu độ 3 hoặc 4.
- Các phản ứng có hại thường thấy nhất xảy ra ở nhóm lenalidomide so với nhóm chứng trong nghiên cứu pha 3 là giảm bạch cầu trung tính (76,8%), giảm tiểu cầu (46,4%), tiêu chảy (34,8%), táo bón (19,6%), buồn nôn. (19,6%), ngứa (25,4%), phát ban (18,1%), mệt mỏi (18,1%) và co thắt cơ (16,7%).
- U lympho tế bào áo choàng
- Hồ sơ an toàn tổng thể của lenalidomide ở bệnh nhân u lympho tế bào lớp áo dựa trên dữ liệu từ 254 bệnh nhân từ nghiên cứu MCL-002 ngẫu nhiên, có đối chứng giai đoạn 2.
- Giảm bạch cầu trung tính (3,6%)
- Thuyên tắc phổi (3,6%)
- Tiêu chảy (3,6%)
- Các phản ứng có hại được quan sát thấy thường xuyên nhất xảy ra ở nhánh lenalidomide so với nhóm đối chứng trong nghiên cứu MCL-002 là giảm bạch cầu trung tính (50,9%), thiếu máu (28,7%), tiêu chảy (22,8%), mệt mỏi (21,0%), táo bón (17,4%), sốt (16,8%), và phát ban (bao gồm cả viêm da dị ứng) (16,2%).
- Trong nghiên cứu MCL-002 nói chung có sự gia tăng rõ ràng về số ca tử vong sớm (trong vòng 20 tuần). Bệnh nhân có gánh nặng khối u cao ở thời điểm ban đầu có nguy cơ tử vong sớm cao hơn, 16/81 (20%) tử vong sớm ở nhóm lenalidomide và 2/28 (7%) tử vong sớm ở nhóm đối chứng. Trong vòng 52 tuần, các con số tương ứng là 32/81 (39,5%) và 6/28 (21%) (xem phần 5.1).
- Giải phẫu hạch bạch huyết
- Giảm bạch cầu do sốt (2,7%)
- Thuyên tắc phổi (2,7%)
- Viêm phổi (2,7%)
- Trong nghiên cứu NHL-007, các phản ứng có hại được quan sát thấy thường xuyên hơn ở nhánh lenalidomide / rituximab so với nhóm giả dược / rituximab (với tần suất cao hơn ít nhất 2% giữa các nhánh) là giảm bạch cầu trung tính (58,2%), tiêu chảy (30,8%), giảm bạch cầu. (28,8%), táo bón (21,9%), ho (21,9%) và mệt mỏi (21,9%).
Tương tác thuốc
- Thuốc uống tránh thai
- Không có nghiên cứu tương tác nào được thực hiện với thuốc tránh thai. Lenalidomide không phải là chất cảm ứng enzym. Trong một nghiên cứu in vitro với tế bào gan người, lenalidomide, ở các nồng độ khác nhau được thử nghiệm không gây ra CYP1A2, CYP2B6, CYP2C9, CYP2C19 và CYP3A4 / 5. Do đó, cảm ứng dẫn đến giảm hiệu quả của các sản phẩm thuốc, bao gồm cả thuốc tránh thai nội tiết tố, không được mong đợi nếu chỉ dùng lenalidomide. Tuy nhiên, dexamethasone được biết là chất cảm ứng CYP3A4 từ yếu đến trung bình và cũng có khả năng ảnh hưởng đến các enzym khác cũng như các chất vận chuyển. Có thể không loại trừ trường hợp hiệu quả của thuốc tránh thai có thể bị giảm trong quá trình điều trị. Phải thực hiện các biện pháp hữu hiệu để tránh mang thai (xem phần 4.4 và 4.6).
- Warfarin
- Sử dụng đồng thời nhiều liều 10 mg lenalidomide không ảnh hưởng đến dược động học liều duy nhất của R- và S- warfarin. Sử dụng đồng thời một liều 25 mg warfarin không ảnh hưởng đến dược động học của lenalidomide. Tuy nhiên, người ta không biết liệu có tương tác trong quá trình sử dụng lâm sàng (điều trị đồng thời với dexamethasone) hay không. Dexamethasone là một chất cảm ứng enzym từ yếu đến trung bình và tác dụng của nó đối với warfarin vẫn chưa được biết rõ. Nên theo dõi chặt chẽ nồng độ warfarin trong quá trình điều trị.
- Digoxin
- Dùng đồng thời với lenalidomide 10 mg x 1 lần / ngày làm tăng 14% phơi nhiễm digoxin trong huyết tương (0,5 mg, liều duy nhất) với KTC 90% (khoảng tin cậy) [0,52% -28,2%]. Người ta không biết liệu tác dụng có khác nhau trong việc sử dụng lâm sàng hay không (liều lenalidomide cao hơn và điều trị đồng thời với dexamethasone). Do đó, nên theo dõi nồng độ digoxin trong khi điều trị bằng lenalidomide.
- Statin
- Tăng nguy cơ tiêu cơ vân khi dùng statin cùng với lenalidomide, có thể chỉ là chất phụ gia. Theo dõi lâm sàng và phòng thí nghiệm tăng cường được đảm bảo đáng chú ý trong những tuần đầu điều trị.
- Dexamethasone
- Sử dụng đồng thời dexamethasone một hoặc nhiều liều (40 mg x 1 lần / ngày) không có ảnh hưởng lâm sàng liên quan đến dược động học của lenalidomide nhiều liều (25 mg x 1 lần / ngày).
- Tương tác với chất ức chế P-glycoprotein (P-gp)
- Trong ống nghiệm , lenalidomide là chất nền của P-gp, nhưng không phải là chất ức chế P-gp. Dùng đồng thời nhiều liều quinidine ức chế P-gp mạnh (600 mg, hai lần mỗi ngày) hoặc temsirolimus / chất ức chế P-gp trung bình (25 mg) không có tác dụng lâm sàng liên quan đến dược động học của lenalidomide (25 mg). Sử dụng đồng thời lenalidomide không làm thay đổi dược động học của temsirolimus.
Quá liều và xử trí
- Không có kinh nghiệm cụ thể trong việc quản lý quá liều lenalidomide ở bệnh nhân, mặc dù trong các nghiên cứu về liều lượng, một số bệnh nhân đã tiếp xúc với liều lên đến 150 mg và trong các nghiên cứu dùng liều đơn, một số bệnh nhân đã tiếp xúc với liều lượng lên đến 400 mg. Độc tính giới hạn liều trong các nghiên cứu này về cơ bản là huyết học. Trong trường hợp quá liều, nên chăm sóc hỗ trợ.
Bảo quản
- Bảo quản ở nhiệt độ không quá 30°C. Tránh ánh sáng. Để xa tầm tay của trẻ em.
Sản phẩm tương tự
Giá thuốc Lenalid 25 là bao nhiêu?
- Lenalid 25 hiện đang được bán sỉ lẻ tại Ung Thư TAP. Các bạn vui lòng liên hệ hotline công ty Call/Zalo: 090.179.6388 để được giải đáp thắc mắc về giá.
Mua thuốc Lenalid 25 ở đâu?
Các bạn có thể dễ dàng mua thuốc Lenalid 25 tại Ung Thư TAP bằng cách
- Mua hàng trực tiếp tại cửa hàng (Liên hệ trước khi tới để kiểm tra còn hàng hay không)
- Mua hàng trên website : https://ungthutap.com
- Mua hàng qua số điện thoại hotline : Call/Zalo: 090.179.6388 để được gặp dược sĩ đại học tư vấn cụ thể và nhanh nhất.
Nguồn tham khảo
- Thông tin về thuốc Lenalid 25 được Ung Thư TAP tổng hợp và sàng lọc kỹ lưỡng và trình bày một cách dễ hiểu nhất. Bạn cũng có thể tham khảo thêm về thông tin thuốc từ:
- https://drugbank.vn/thuoc/Soravar&QL%C4%90B-773-19
Câu hỏi thường gặp
Ung thư TAP hiện nay là một trong những website bán Lenalid 25 (Lenalidomide 25mg) - Thuốc trị đa u tủy hiệu quả chính hãng mà quý khách hàng có thể tin tưởng và đặt mua hàng. Để mua hàng tại Ung thư TAP, bạn có thể lựa chọn một trong các cách thức như sau:
- Mua hàng trực tiếp tại cửa hàng theo khung giờ sáng:9h-11h30, chiều: 2h-4h.
- Đặt hàng và mua trên website : https://ungthutap.com
- Gọi điện qua số điện thoại Hotline 0971.899.466 hoặc nhắn tin qua Zalo: 090.179.6388 để được gặp dược sĩ đại học tư vấn cụ thể và nhanh nhất.
Tuyên bố miễn trừ trách nhiệm:
Tất cả các thông tin được cung cấp trên trang web này chỉ là những thông tin tổng quan, không được xem là tư vấn y khoa và không nhằm mục đích thay thế cho việc tư vấn, chẩn đoán từ bác sĩ hay các chuyên viên y tế. Chúng tôi luôn nỗ lực để có thể cập nhật những thông tin mới và chính xác đến người đọc. Đồng thời, chúng tôi cũng không tuyên bố hay bảo đảm dưới bất kỳ hình thức nào, rõ ràng hay ngụ ý, về tính chất đầy đủ, chính xác, kịp thời, đáng tin cậy, phù hợp hoặc sẵn có với những thông tin, sản phẩm, dịch vụ hoặc hình ảnh, hay các thông tin trong văn bản có liên quan và tất cả các tài liệu khác có trên website cho bất kỳ mục đích nào. Chính vì vậy, bạn đọc không thể áp dụng cho bất kỳ tình trạng y tế của cá nhân nào và có thể sẽ xảy ra rủi ro cho người đọc khi dựa vào những thông tin đó.
Sản phẩm liên quan
Sản phẩm cùng hãng
Bình luận
Bạn hãy là người đầu tiên nhận xét về sản phẩm này